Menganalisis Produk Korosi Berair

Kombinasi beberapa metode sering diperlukan untuk mengidentifikasi produk korosi berair dengan benar dengan metode yang paling umum digunakan adalah pemindaian mikroskop elektron (SEM-EDS) / spektroskopi sinar-X dispersif energi (XRD). Identifikasi produk korosi penting untuk mencegah kejadian di masa depan dan akan berdampak pada keputusan baik mengubah metalurgi atau memodifikasi kondisi proses. Berikut ini adalah beberapa produk korosi berair yang diharapkan untuk berbagai paduan dan kondisi.
Diagram Pourbaix
Diagram Pourbaix dapat menjadi alat yang berguna untuk menentukan produk korosi berair yang diantisipasi, yang kemudian dapat dibandingkan dengan yang diamati. Kesetimbangan termodinamika digunakan untuk memprediksi stabilitas fasa dalam sistem yang dikontrol secara elektrokimia. Diagram Pourbaix mirip dengan diagram fase yang menunjukkan batas stabilitas untuk sistem logam-berair di mana stabilitas fase terkait dengan pH dan potensial elektronik hidrogen standar.
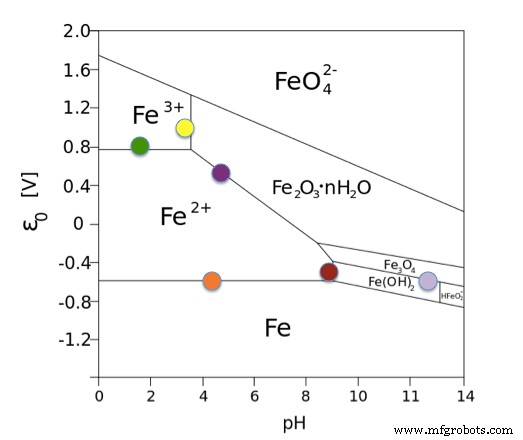 Diagram Pourbaix untuk Fe.
Diagram Pourbaix untuk Fe.
Sumber:Andel Früh, Wikimedia Commons
Diagram ini sangat berguna untuk mengidentifikasi di mana logam mungkin aktif atau pasif terhadap korosi. Dengan munculnya data termodinamika yang ditingkatkan, diagram paduan Pourbaix menggunakan metodologi CALPHAD tersedia dan dapat digunakan untuk menunjukkan potensi korosi atau spesies skala pelindung. Mereka dapat membantu dalam memahami produk korosi yang diamati berdasarkan keadaan oksidasi spesies yang diprediksi dalam larutan dan skala pelindung yang diantisipasi. Jika ada inkonsistensi, maka kondisi proses atau kimia korosi tidak ditentukan dengan benar.
Energy Dispersive Spectroscopy (EDS)
Baru-baru ini, spektroskopi dispersi energi (EDS) telah digunakan untuk mengidentifikasi produk korosi, tetapi metode ini juga memiliki kekurangan yaitu hanya mengidentifikasi unsur, bukan senyawa. Senyawa harus disimpulkan dengan EDS, yang hampir tidak mungkin jika sampel memiliki beberapa bentuk besi sulfida. Dengan demikian, metode ladang minyak sederhana yang sering digunakan untuk identifikasi produk korosi seringkali menyesatkan. Mereka tidak boleh diandalkan untuk membuat keputusan serius mengenai kondisi peralatan atau penyebab korosi dalam suatu sistem. Difraksi sinar-X (XRD) harus digunakan untuk mengidentifikasi dan memahami secara positif produk korosi yang ada.
Besi-Baja Ringan
Besi dan baja ringan dalam air akan menghasilkan produk korosi magnetit yang tidak larut (Fe3 O4 ), lepidokrosit (g-FeOOH) dan goetit (a-FeOOH) tergantung pada pH. Jumlah masing-masing konstituen dapat bervariasi dengan suhu. Larutan asam 200 ppm klorida yang diangin-anginkan pada 25°C (77°F), seperti dari pelapukan, menghasilkan lapisan karat yang terdiri dari hematit (a-Fe2 O3 ) dan magnetit.
Beberapa perbedaan dalam produk korosi telah dicatat jika permukaan baja terkena uap HCl yang lebih pekat atau dalam larutan HCl. Pada paparan uap pekat HCl yang lebih rendah, campuran goetit dan akageneit (b-FeOOH) diamati; sedangkan pada konsentrasi uap HCl yang lebih tinggi FeCl2 · 4H2 O ditemukan. Paparan baja terhadap larutan HCl menghasilkan lepidokrosit, goetit dan hematit. Sedangkan produk korosi yang dicatat untuk baja dalam air laut antara lain akageneite, goethite dan FeOCl. Jadi, Kl
-
produk korosi dapat sangat bervariasi tergantung pada kondisi paparan. Bila kandungan Cr>4%, kandungan Cr dapat mendorong konversi magnetit menjadi goetit pada lapisan karat.
Kehadiran SO4
=
menghasilkan produk korosi lepidokrosit, magnetit, hematit dan goetit dan dengan waktu yang lebih singkat ferrihidrit (Fe5 O7 (OH)· 4H2 O), yang tidak terlalu stabil secara termal dan mudah berubah menjadi goetit dan hematit.
CO2 encer2 korosi cenderung menghasilkan FeCO3 endapan pada suhu yang lebih rendah. Pada suhu di atas 100°C (212°F) kedua FeCO3 dan magnetit diamati, tetapi yang mendominasi adalah fungsi dari tekanan parsial CO2 . Dalam larutan karbonat, spesies amorf dan ferihidrit, hematit, kemungkinan FeCO3 dan besi hidroksi karbonat (Fe2 (OH)2 CO3 ) dapat diamati.
Untuk H2 aqueous berair S, mackinawite (FeS) adalah besi sulfida yang paling tidak stabil secara termodinamika tetapi memiliki kinetika pembentukan tercepat. Setelah awalnya terbentuk sebagai lapisan tipis pada logam, ia dapat berubah menjadi bentuk sulfida besi lain yang lebih stabil, seperti pirhotit (Fe1-x S) dan pirit (FeS2 ). Pada 25°C (77°F) mackinawite, greigite (Fe3 S4 ) dan pirhotit diamati, sedangkan pada 80°C (176°F) mackinawite, pirhotit dan pirit terdeteksi.
Studi lain pada 120 ° C (248 ° F) mencatat bahwa dengan waktu mackinawite berubah menjadi troilite (FeS) dan kemudian menjadi pirhotit dan dengan waktu lebih lanjut menjadi pirit. Dengan tidak adanya O2 dan Cl, FeS kubik mungkin merupakan sulfida perantara. Sisik sulfida ini juga dapat diamati sebagai lapisan korosi pada logam. Kombinasi dari campuran H2 S/CO2 larutan cenderung mengubah lapisan pirhotit menjadi troilite dan beberapa mackinawite. Dengan demikian, pertumbuhan dan transisi fase besi sulfida polimorf dengan rasio dan struktur stoikiometrik Fe/S yang berbeda sangat kompleks dan merupakan fungsi dari kondisi paparan.
Dalam larutan NaOH, hematit cenderung menjadi produk korosi yang dominan.
Dalam kondisi reduksi, magnetit akan terbentuk pada permukaan sisi air boiler. Hematit disukai pada suhu yang agak lebih rendah dan konsentrasi oksigen yang lebih tinggi.
Baja Tahan Karat Austenitik
Untuk paduan ini, Cr yang seragam dengan ketebalan 1-3 nm2 O3 film pasif permukaan logam dan meminimalkan pewarnaan dan korosi. Jika lapisan pelindung ini larut dan/atau rusak, maka korosi dapat terjadi dengan korosi yang cenderung menjadi serangan pitting. (Bacaan terkait:Mencegah Korosi Pewarnaan Teh pada Stainless Steel.)
Karena jumlah produk korosi yang terbatas, sebagian besar identifikasi spesies korosi dicapai dengan SEM-EDS. Analisis XRD endapan dari korosi HCl mengungkapkan FeCl2 , hematit dan Cr2 O3 . Paparan air laut dapat menghasilkan hematit, magnetit dan Fe(CrO4 )OH. Untuk paduan Ni yang lebih tinggi seperti 904L dalam HF, endapan terdiri dari NiF2 , hematit dan Cr2 O3 . Dalam asam sulfat Tipe 304 menghasilkan lapisan pasif oksihidroksida, hematit, FeO, NiO, sulfat, sulfit dan Fe dan Ni sulfida.
Paduan Tembaga dan Tembaga
Larutan berair akan mengoksidasi tembaga murni dengan Cu2 O (cuprite) menjadi produk utama yang tidak larut dengan Cu
+2
menjadi spesies yang paling mudah larut. Adanya klorida akan meningkatkan kelarutan Cu(I) sehingga CuCl2
-
menjadi spesies larut yang dominan. Dalam lingkungan laut, cuprite awalnya terbentuk; interaksi lebih lanjut dengan Cl
-
menghasilkan nantokite (CuCl), yang kemudian dapat berubah menjadi atacamite atau paratacamite fase isomorf (Cu2 (OH)3 Cl) sebagai produk korosi patina akhir.
Di lingkungan yang tercemar belerang, tembaga pada awalnya akan terbentuk tetapi mungkin juga ada Cu4 JADI4 (OH)6
.
H2 O, Cu4 JADI4 (OH)6 (brochantite), dan Cu3 JADI4 (OH)4 dalam produk korosi. Jika H2 S hadir dalam lingkungan pereduksi seperti dalam kasus korosi yang disebabkan oleh mikroba (MIC), CuS atau Cu8 S5 mungkin terjadi.
Cu dan Zn adalah elemen utama dalam keluarga paduan kuningan. Karena perbedaan potensial keseimbangan Cu dan Zn yang cukup besar, dealloying Zn dapat terjadi di lingkungan berair yang mengakibatkan lapisan terdeplesi Zn dan produk korosi Cu dan Zn. Biasanya ini termasuk cuprite, CuO, Cu(OH)2 , ZnO dan Zn(OH)2 . Di lingkungan laut, seng hidrokarbonat amorf, Zn5 (CO3 )2 (OH)6 dan ZnO dapat diamati.
Paduan Sn ke Cu menghasilkan keluarga paduan perunggu. Dalam media berair, SnO2 film bisa semi-pasif. Lapisan cuprite yang rusak kemudian dipisahkan dari paduan curah dengan pelindung dalam SnO2 . Di hadapan Kl
-
nantokite luar kadang-kadang terbentuk tetapi dengan waktu yang lebih lama di lingkungan laut CuO, Cu2 CO3 (OH)2 dan atacamite dapat diproduksi dan di perairan tercemar brochantite juga mungkin ada.
Paduan nikel tembaga dikenal karena ketahanannya terhadap korosi. Dalam lingkungan laut cuprite akan cepat terbentuk pada awalnya dan berpotensi menjadi pelindung; tetapi dengan paparan Cl
-
, nantokite, CuCl2 dan paratacamite diproduksi. Dalam sulfida aerasi yang mengandung air laut, spesies yang paling signifikan adalah Cu2 S dengan campuran nantokite, NiS, cuprite dan NiO. (Bacaan terkait:11 Penggunaan Cupronickel dan Mengapa Anda Harus Menggunakannya Sekarang.)
Paduan Nikel
Paduan berbasis nikel dipilih untuk lingkungan korosif yang agresif di mana baja tahan karat tidak cocok. Dengan paduan Ni dengan berbagai jumlah Cr dan Mo dan sejumlah kecil W, Cu dan Fe, ketahanan korosi yang tinggi dapat dicapai. Film pasif tipis terdiri dari bagian dalam Cr2 O3 lapisan kaya dan lapisan luar Cr/Ni hidroksida dan Mo/Cu atau W, yang memberikan perlindungan korosi. Analisis difraksi elektron menunjukkan bahwa gugus ini adalah Ni1-x Cr2x/3 O dan b-Ni1-x Cr2x/3 (OH)2 dengan Mo mungkin menggantikan beberapa Cr.
Dalam kondisi agresif, cacat pada film pelindung dapat menyebabkan kerusakan lokal dan tanpa re-passivation, pelarutan logam dapat terjadi dengan korosi lubang atau celah berikutnya. Produk korosi di dalam celah untuk Paduan 22 yang terpapar air garam klorida panas ditemukan sebagai MoO2 dan Mo4 O11; W dapat diganti dalam molibdat atau sebagai spesies oksida terpisah.





 Diagram Pourbaix untuk Fe.
Diagram Pourbaix untuk Fe.