Defosforisasi Baja
Defosforisasi Baja
Efek fosfor (P) pada sifat baja dirangkum dalam Tab 1. Dapat dilihat bahwa P memiliki efek positif dan negatif pada sifat baja.
| Tab 1 Pengaruh fosfor pada sifat baja |
| | |
| No.Sl. | Properti | Efek fosfor |
| | |
| 1 | Kekuatan | Positif kuat (memperkuat ferit) |
| 2 | Kemampuan memanggang roti | Positif |
| 3 | Daktilitas | Negatif kuat |
| 4 | Galvanneal | Dapat meningkatkan ketahanan terhadap bedak |
| 5 | Phosfatabilitas | Positif |
| 6 | Email | |
| a. Sisik ikan | Negatif |
| b. Pengasinan | Positif |
| 7 | Kemampuan las | Tidak berbahaya untuk konten kurang dari 0,1 % |
| 8 | Kehilangan inti pada laminasi motor | Negatif kuat |
| 9 | Ketangguhan retak | Negatif kuat |
Baja dengan kandungan P rendah diperlukan untuk aplikasi di mana daktilitas tinggi diperlukan, seperti lembaran tipis, baja yang ditarik dalam, dan jaringan pipa dll. Pada hari-hari sebelumnya, kontrol P tidak dianggap sebagai tantangan besar dalam produksi baja karena bijih besi dengan kandungan P rendah. Isi P tersedia dengan mudah dan murah. Namun, belakangan ini, karena harga bijih besi yang tinggi, bijih besi dengan harga lebih rendah dari sumber yang biasanya memiliki kandungan P lebih tinggi digunakan dan hal ini membuat pengendalian P menjadi aktivitas penting selama pembuatan baja.
Selain P dari dalam bijih besi, P juga masuk ke dalam baja cair karena daur ulang terak BOF (basic oxygen furnace). Daur ulang terak BOF sedang dilakukan melalui pabrik sinter atau langsung ke tanur sembur untuk mengambil kandungan besi dan kapur dari terak dan untuk meminimalkan masalah yang terkait dengan pembuangan terak. Sinter atau terak BOF yang diumpankan ke tanur sembur pasti meningkatkan kandungan P dari logam panas dan karenanya beban P pada proses pembuatan baja.
Di pabrik baja terintegrasi, penghilangan P biasanya terjadi selama proses pembuatan baja utama biasanya proses BOF. Untuk memenuhi tuntutan baru untuk kontrol P, perlu untuk meningkatkan pemahaman tentang termodinamika dan kinetika reaksi partisi P antara terak dan lelehan logam selama proses pembuatan baja.
Defosforisasi baja telah menjadi teknik metalurgi yang sangat penting dalam proses pembuatan baja untuk menghasilkan baja berkualitas tinggi. Karena kandungan P dikendalikan oleh reaksi dalam BOF, teknik terak ganda umumnya diterapkan untuk mendapatkan baja mati P rendah. Namun, teknik ini disertai dengan peningkatan waktu operasi dan penurunan yield baja. Selain masalah produktivitas dengan teknik ini, sejumlah besar BOF slag juga dihasilkan selama pengoperasian BOF.
Fosfor juga dapat dihilangkan selama proses pemurnian baja. Faktanya, lebih dari 90% input P dalam lelehan dapat dihilangkan di BOF. Kapasitas pemurnian terak tergantung dari banyak variabel seperti komposisi terak dan logam, suhu, waktu dan intensitas pengadukan terak/logam.
Kandungan P dalam baja cair selama penyadapan, deoksidasi, peniupan gas inert, dan pengecoran dapat meningkat secara bertahap karena pengenalannya dengan deoksidasi dan reduksi dari terak. Kemungkinan ini harus diperhitungkan untuk menjaga kondisi defosforisasi dalam baja cair. Sebagai hasil reaksi antara baja, terak, dan deoxidizers, kesetimbangan P bergeser ke arah peningkatan kandungan P dalam baja meskipun terjadi penurunan suhu yang signifikan. Dalam hal ini, defosforisasi sangat bergantung pada rasio baja terhadap berat terak. Peran faktor-faktor tersebut dapat disimpulkan dari persamaan keseimbangan P berikut.
(Kandungan P dalam terak sendok) + (Kandungan P dalam sendok baja) =(Kandungan P dalam logam yang disadap) + (Kandungan P dalam terak yang terperangkap oleh baja dalam sendok) + (P dari deoksidasi).
Reaksi fosfor dan kesetimbangan termodinamika
Studi komprehensif awal tentang defosforisasi dilakukan selama tahun 1940-an. Studi-studi ini mengamati bahwa FeO dan CaO adalah konstituen terak yang diperlukan untuk defosforisasi baja. Studi-studi ini juga menunjukkan bahwa reaksi defosforisasi adalah eksotermik dan bahwa kapasitas terak untuk defosforisasi menurun dengan suhu. Studi juga mengamati bahwa defosforisasi ditingkatkan dengan penurunan suhu dan peningkatan kandungan FeO dan kebasaan terak.
Banyak korelasi telah dikembangkan untuk memprediksi rasio partisi P sebagai fungsi komposisi logam dan terak serta suhu. Namun, masih ada ketidaksepakatan dalam data laboratorium dan partisi P kesetimbangan yang dapat diprediksi.
Meskipun kuantifikasi kesetimbangan P sangat penting, banyak tungku pembuatan baja tidak beroperasi pada kesetimbangan, biasanya karena pembentukan terak cair, kinetika dan kendala waktu. Oleh karena itu, penting untuk mengetahui seberapa dekat tungku pembuatan baja kesetimbangan beroperasi untuk menyarankan komposisi terak yang optimal untuk mendorong defosforisasi.
Telah dicatat selama studi awal bahwa kondisi pengadukan dan komposisi terak adalah dua variabel kunci untuk memungkinkan penyisihan P yang optimal. Juga, terlalu jenuhnya terak dengan CaO dan MgO tampaknya tidak menguntungkan proses sampai batas tertentu.
Ditemukan selama studi ini bahwa fenomena antarmuka dinamis pada antarmuka terak logam kemungkinan memainkan peran penting dalam perilaku kinetik sistem, karena pertukaran elemen aktif permukaan, seperti oksigen (O2), yang secara dramatis menurunkan tegangan antarmuka dan menyebabkan emulsifikasi spontan. Ditemukan juga bahwa P tidak berperan dalam emulsifikasi spontan dan dengan cepat dihilangkan sebelum timbulnya fenomena antarmuka dinamis. Emulsifikasi mungkin disebabkan oleh deoksidasi logam setelah penghilangan P terjadi dan logam menjadi sangat jenuh dengan O2 dengan alasan yang tidak diketahui. Luas permukaan yang diperkirakan meningkat dengan cepat melebihi urutan besarnya selama periode awal dan pertengahan reaksi. Tetesan logam pecah menjadi ratusan tetesan kecil, secara efektif mengemulsi logam menjadi terak. Seiring waktu, luas permukaan berkurang dan tetesan logam menyatu. Hasil serupa diamati untuk tetesan besi (Fe) yang dioksidasi.
Pada tahun 1950-an, diusulkan bahwa reaksi yang berlangsung dalam bentuk yang paling sederhana seperti yang diberikan di bawah ini memuaskan.
2P + 5O =P2O5 (cair)
Energi bebas yang terkait dengan reaksi dievaluasi menggunakan perkiraan entropi fusi P2O5, sehingga
Delta G =– 740375+535.365T J/mol
Pada T lebih dari 1382 derajat K, Delta G? menjadi positif yang mengakibatkan penguraian P2O5 menjadi P dan O. Dengan demikian penyisihan P memerlukan P2O5 perlu direduksi. Koefisien aktivitas P2O5 meningkat dengan silika (SiO2) dan menurun dengan oksida basa seperti CaO dan MgO.
Selama tahun 1980-an studi lebih lanjut dilakukan pada partisi P di berbagai sistem terak. Studi-studi ini telah menunjukkan bahwa rasio distribusi P meningkat dengan meningkatnya kandungan CaO dalam terak dan dengan penurunan suhu. Terlihat juga bahwa efek CaF2 pada defosforisasi sama dengan CaO tanpa menaikkan titik leleh terak. Efek barium oksida (BaO) dan natrium oksida (Na2O) pada partisi P juga dipelajari. Studi-studi ini menyimpulkan bahwa kesetaraan CaO dari Na2O dan BaO masing-masing adalah 1,2 dan 0,9 persen berat.
Distribusi P dalam sistem terak yang berbeda telah dipelajari berkali-kali dan beberapa korelasi telah dikembangkan. Berbagai kesimpulan dari studi ini dirangkum di bawah ini.
- Kandungan CaO, MgO, SiO2, P2O5, FeO, dan MnO dari terak berpengaruh terhadap partisi P.
- Terak cair sepenuhnya terionisasi dan P dalam terak ada sebagai ion fosfat.
- Log dari partisi P meningkat dengan 2,5 log % FeO seperti yang diprediksi oleh termodinamika dan bahwa peningkatan kebasaan terak juga meningkatkan koefisien partisi.
- Meningkatkan kebasaan terak (CaO/SiO2) hingga 2,0 memiliki efek peningkatan yang kuat pada partisi P. Namun, peningkatannya jauh lebih kecil dengan dasar di atas 2,5.
- Rasio partisi P awalnya meningkat dengan meningkatnya kandungan FeO tetapi kemudian menurun setelah tingkat tertentu tercapai. Tingkat ini merupakan fungsi dari kebasaan terak dan suhu. Kesimpulan ini juga berlaku untuk kandungan FeO dalam terak antara 15% dan 25%. Lebih khusus lagi, partisi P tidak tergantung pada kandungan FeO di atas 19%. Selain itu, partisi P tampak lebih rendah dengan peningkatan kandungan MgO pada suhu 1600 derajat C dan 1650 derajat C.
- Untuk terak yang mengandung P2O5 dari 0,2 % hingga 1,0% log dari koefisien aktivitas P2O5 adalah fungsi linier dari kandungan CaO dan MgO dan tidak ada ketergantungan suhu. Untuk slag yang mengandung P2O5 lebih dari 1% log dari koefisien aktivitas P2O5 juga merupakan fungsi linier dari CaO tetapi juga memiliki ketergantungan suhu.
- Peningkatan konsentrasi Ca2+, Fe2+ dan Mg2+ mengakibatkan penurunan koefisien aktivitas P2O5 sedangkan (SiO4)4- memiliki efek sebaliknya.
- Polimerisasi P tidak terjadi secara ekstensif pada terak yang biasanya ditemukan dalam pembuatan baja.
Pendekatan lain untuk partisi model P antara baja dan terak juga telah dicoba. Pada tahun 2011, model termodinamika lengkap berdasarkan teori koeksistensi ion dan molekul (IMCT) telah dikembangkan untuk memprediksi rasio distribusi P antara terak CaO-SiO2-FeO-Fe2O3-MnO-Al2O3-P2O5 dan baja cair. IMCT mengasumsikan bahwa terak terdiri dari ion sederhana, seperti Ca2+, Fe2+, Mg2+ dan O2-; molekul sederhana, P2O5, SiO2 dan Al2O3; silikat, aluminat dan banyak lainnya sebagai molekul kompleks. Setiap spesies ionik mengambil bagian dalam reaksi untuk membentuk molekul kompleks dari pasangan ion (Me2+ dan O2-) dan molekul sederhana dan berada di bawah kesetimbangan termodinamika. Kemungkinan molekul P yang diperhitungkan adalah P2O5, 3FeO.P2O5, 4FeO.P2O5, 2CaO.P2O5, 3CaO.P2O5, 4CaO.P2O5, 2MgO.P2O5, 3MgO.P2O5 dan 3MnO.P2O5. Telah ditemukan bahwa 3CaO.P2O5 dan 4CaO.P2O5 memiliki kontribusi terhadap partisi P terukur masing-masing sebesar 96 % dan 4%.
Diskusi sejauh ini melibatkan keseimbangan P antara baja cair dan terak cair. Namun, karena sifat multikomponen dari pembuatan baja terak, tidak jarang memiliki fase padat yang mungkin dalam kesetimbangan dengan terak cair. Studi substansial telah dilakukan pada fase padat tertentu yang umum dalam pembuatan baja terak. Lebih khusus, penelitian telah difokuskan pada terak yang mengandung partikel 2CaO.SiO2 dan CaO. Fase padat ini biasanya terdapat dalam slag pembuatan baja selama proses BOF dan dapat berperan dalam defosforisasi karena fosfat dapat larut di dalamnya.
Pemurnian fosfor dalam proses BOF
Pembuat baja yang baik juga pembuat terak yang baik' adalah pepatah populer di kalangan personel pembuat baja dan sangat relevan dalam konteks proses BOF. Memiliki kontrol yang baik atas pembentukan dan komposisi terak memungkinkan pemurnian optimal dan meminimalkan risiko harus meniup ulang O2 atau membuat tambahan ekstra di akhir pemanasan. Selama awal pukulan, tombak dijaga tetap tinggi di atas permukaan logam. Selama 3 sampai 4 menit pertama Si (silikon) dari logam dengan cepat teroksidasi bersama dengan Fe membentuk terak yang kaya akan FeO dan SiO2. Sejumlah besar kapur dan kapur dolomit ditambahkan ke dalam BOF. Saat pukulan berlanjut, kapur padat terus menerus larut ke dalam terak cair meningkatkan massa dan kebasaan terak. Saat dekarburisasi berlanjut, terak mulai berbusa dan gas CO yang dihasilkan mengurangi kandungan FeO dalam terak. Menjelang akhir pukulan, laju dekarburisasi menurun dan oksidasi Fe menjadi signifikan lagi. Sepanjang pukulan suhu logam terus meningkat dari 1350 derajat C menjadi 1650 derajat C dan suhu terak umumnya 50 derajat C lebih tinggi dari logam pada akhir pukulan.
Mekanisme pelarutan kapur sangat relevan dengan proses BOF dan penyisihan P. Pencapaian pelarutan kapur yang cepat selama proses BOF memberikan peluang yang baik untuk meningkatkan produktivitas, mengurangi waktu dan biaya proses. Mekanisme pelarutan kapur merupakan fungsi dari komposisi terak dan tingkat kejenuhan dikalsium silikat (2CaO.SiO2). Terak awal kaya akan FeO dan SiO2. Ketika kapur pertama kali ditambahkan dan mulai larut, lapisan 2CaO.SiO2 terbentuk di sekitar partikel padat dan memperlambat laju pelarutan kapur. Lapisan padat ini dapat pecah dan terak selanjutnya dapat menembus pori-pori partikel kapur dan melanjutkan pelarutan. Penetrasi terak adalah fungsi dari viskositas dan ukuran pori dari partikel padat.
Karena dalam proses BOF sering ada beberapa fase oksida padat yang hidup berdampingan dengan terak, penting untuk memahami bagaimana partikel padat dapat mempengaruhi penyisihan P. Beberapa penelitian telah melihat kelarutan P dalam partikel padat yang berbeda seperti CaO, 2CaO.SiO2 dan 3CaO.SiO2. Berikut ini adalah beberapa kesimpulan dari penelitian tersebut.
- Partisi fosfor antara partikel 2CaO.SiO2 dan terak bervariasi antara 2 hingga 70 seiring dengan meningkatnya kandungan FetO dan kebasaan dalam terak. Ketergantungan suhu pada distribusi P ditemukan sangat lemah dan partikel terisolasi 2CaO.SiO2 menunjukkan transformasi seragam lengkap menjadi 2CaO.SiO2-3CaO.P2O5 dalam waktu 5 detik.
- Setelah kontak dengan terak CaO-FetO-SiO2-P2O5, partikel CaO dengan cepat dienkapsulasi oleh lapisan 2CaO.SiO2-3CaO.P2O5 dan terak CaO-FetO tanpa P2O5 terbentuk antara partikel CaO dan 2CaO .SiO2-3CaO.P2O5 larutan padat.
- Ada dua kemungkinan rute untuk transfer P dari terak ke 2CaO.SiO2. Pada rute pertama, 2CaO.SiO2-3CaO.P2O5 akan mengendap dari terak cair setelah P dipindahkan dari fasa logam. Pada kemungkinan rute kedua, partikel 2CaO.SiO2 sudah ada dalam terak sebelum P dipindahkan dari logam. P kemudian berdifusi ke dalam partikel 2CaO.SiO2 bebas P yang diendapkan. Telah ditemukan bahwa laju transfer P melalui jalur presipitasi jauh lebih cepat daripada jalur difusi. Ini menunjukkan fakta bahwa memiliki partikel 2SiO2.SiO2 yang sudah ada sebelumnya tidak serta merta meningkatkan penyisihan P.
Selama pukulan dalam proses BOF, lingkungan yang sangat dinamis tercipta. Saat pancaran O2 mengenai permukaan terak dan, selanjutnya, logam cair, ia menciptakan emulsi tiga fase gas-terak-logam, yang secara signifikan meningkatkan total luas antarmuka yang tersedia untuk beberapa reaksi kimia yang terjadi di antara fase. Tetesan logam terus menerus dikeluarkan dari rendaman logam curah ke dalam campuran terak-gas di mana mereka dapat bereaksi untuk waktu tertentu. Pembentukan tetesan logam ini sangat penting untuk kinetika di dalam BOF.
Laju pemurnian, selama proses BOF, tidak hanya merupakan fungsi dari kinetika kimia tetapi juga fungsi dari waktu tinggal yang dikeluarkan oleh tetesan logam tertentu dalam terak. Waktu tinggal yang dihitung dari tetesan logam yang dikeluarkan dari logam curah yang bergerak dalam lintasan balistik melintasi terak kurang dari 1 detik yang terlalu pendek untuk tetesan tertentu untuk bereaksi sampai batas yang signifikan. Namun, selama studi tentang perilaku tetesan Fe-C dalam terak, telah diamati bahwa pembentukan 'halo' gas saat dekarburisasi terjadi, membuat tetesan logam tersuspensi dalam terak dari 50 detik menjadi 200 detik. Berdasarkan pengamatan ini, model dimodifikasi untuk memasukkan efek dekarburisasi pada densitas nyata dari tetesan logam dan mampu memprediksi waktu tinggal yang konsisten.
Laporan berjudul 'Imphos:Meningkatkan Pemurnian Fosfor' yang diterbitkan pada tahun 2011 telah melihat, antara lain, pada profil rasio logam/terak, distribusi ukuran tetesan logam dalam emulsi terak/logam, distribusi P pada antarmuka terak-logam, dan pelarutan kapur. Laporan tersebut telah mendefinisikan lima profil penghilangan P seperti yang ditunjukkan pada Gambar 1. Profil ini adalah (i) profil P mendekati konstan, (ii) profil pembalikan P, (iii) profil penghilangan P tinggi, (iv) profil pembalikan dan perlambatan P, dan (v) pembalikan dengan profil penghilangan P cepat. Untuk masing-masing profil ini, jumlah logam dan komposisi kimianya telah dipelajari untuk emulsi terak/logam dan untuk rendaman curah. Telah ditemukan bahwa kandungan P dari tetesan logam dalam terak biasanya lebih rendah dari atau sama dengan rendaman curah, menunjukkan fakta bahwa penghilangan P didorong oleh defosforisasi tetesan logam yang ada dalam emulsi terak/logam daripada dalam emulsi terak/logam. mandi massal. Satu pengamatan menarik dalam laporan tersebut adalah bahwa, selama tahap awal pukulan, penghilangan P dalam tetesan emulsi terjadi jauh lebih cepat daripada dekarburisasi.
Tetesan logam ditemukan sangat terkuras dalam P (kurang dari 100 ppm) sementara ada lebih dari 1% C di bak mandi. Hal ini berpotensi terkait dengan gas 'halo' dan emulsifikasi, yang dapat meningkatkan waktu tinggal tetesan selama tahap awal pukulan sehingga memberikan waktu yang cukup untuk bereaksi dengan terak pengoksidasi tinggi yang ada, menghasilkan penghilangan P yang cepat jika ukuran tetesan sesuai. Karena penghilangan P sangat terkait dengan pembentukan tetesan logam, ada ketinggian tombak yang ideal selama setiap tahap pukulan untuk memaksimalkan pembentukan tetesan dan menciptakan emulsi terak/logam/gas yang baik. Diamati bahwa saat ketinggian tombak berkurang, lebih sedikit tetesan logam yang dihasilkan.
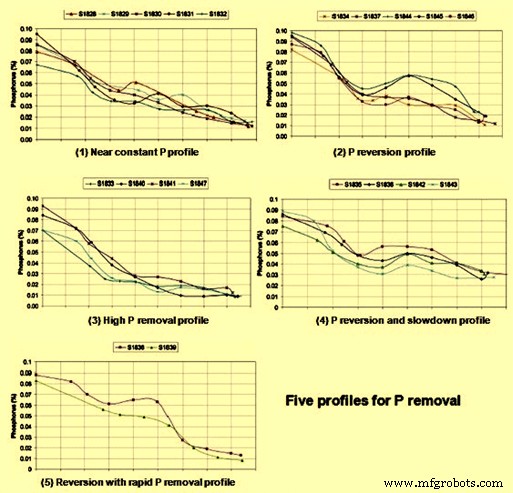
Gbr 1 Berbagai profil penghapusan P
Mekanisme defosforisasi dalam proses BOF dapat diringkas sebagai berikut.
- Selama awal pukulan, di mana tombak O2 dijaga tetap tinggi, ejeksi tetesan yang baik tercapai dan pelepasan P terjadi dengan cepat.
- Saat pukulan berlanjut dan dekarburisasi mulai menghasilkan gas CO, FeO dalam terak berkurang dan terak menjadi tidak cukup teroksidasi. Hal ini dapat mengakibatkan pengembalian P ke dalam lelehan karena tetesan difosforisasi ulang dan kembali ke logam curah. Ini sangat penting jika pembubaran kapur tidak optimal.
- Mendekati akhir pukulan, dekarburisasi melambat dan kandungan FeO dalam terak meningkat mendukung defosforisasi sekali lagi. Namun, ini mungkin tidak cukup untuk mengkompensasi kemungkinan pengembalian yang terjadi sebelumnya.
- Hasil optimal dapat dicapai dengan memonitor FeO dan CaO dalam slag. Penambahan bijih besi dapat membantu mempertahankan kandungan FeO yang ideal untuk melanjutkan oksidasi P secara paralel dengan dekarburisasi.
Kinetika penghilangan fosfor
Meskipun keseimbangan P telah dipelajari secara luas, kinetika penyisihan P belum dipelajari sejauh itu. Namun, prinsip yang sama untuk reaksi metalurgi suhu tinggi lainnya berlaku. Ketika P dilarutkan dalam terak kontak Fe, beberapa langkah yang memberikan ilustrasi dasar dari fenomena tersebut, berlangsung selama reaksi defosforisasi. Langkah-langkah tersebut adalah sebagai berikut.
- Perpindahan massa dalam fasa logam [P] dan [O] menuju antarmuka terak-logam
- Perpindahan massa dalam fase terak (O2-) menuju antarmuka terak-logam
- Reaksi kimia pada antarmuka terak-logam untuk pembentukan (PO4)3-
- Perpindahan massa dalam fase terak (PO4)3- menjauh dari antarmuka reaksi
Karena defosforisasi terjadi pada suhu tinggi, masuk akal untuk mengasumsikan bahwa reaksi kimia pada antarmuka berlangsung cepat dan pada kesetimbangan. Oleh karena itu, langkah pembatas laju yang mungkin adalah perpindahan massa dalam logam atau fase terak atau keduanya, jika diasumsikan bahwa tidak ada fase padat dalam terak yang mampu menyerap fosfor.
Salah satu studi tentang kinetika defosforisasi logam panas Fe-C(sat)-P dengan mengoksidasi terak, menunjukkan bahwa salah satu tantangan utama dalam defosforisasi logam cair adalah mengukur dengan tepat gaya penggerak reaksi akibat non -keseimbangan potensial O2 pada antarmuka terak/logam. Ketidak seimbangan ini terjadi karena dekarburisasi logam cair yang menurunkan potensial O2 dalam logam. Dalam kasus seperti itu, terak berada pada potensial O2 tinggi sedangkan logam pada potensial O2 rendah. Selama penelitian telah ditemukan bahwa reaksi defosforisasi mengikuti laju kinetik orde pertama sehubungan dengan konsentrasi P dalam logam dan kandungan FeO yang lebih tinggi meningkatkan koefisien perpindahan massa terak karena penurunan viskositas, meskipun FeO juga dapat berdampak positif atau negatif kekuatan pendorong reaksi. Studi ini juga menunjukkan bahwa transportasi massal dalam fase terak adalah langkah pembatas laju dalam defosforisasi logam.
Baru-baru ini, penelitian lain menggunakan pendekatan matematis untuk mengukur perpindahan massa P antara logam dan terak. Studi telah menunjukkan bahwa koefisien perpindahan massa yang tampak tampaknya menjadi fungsi dari tegangan antarmuka, yang dipengaruhi oleh fluks massa elemen aktif permukaan, seperti O2, terutama di bawah kondisi perpindahan massa yang cepat. Perubahan parameter perpindahan massa terkait dengan fenomena antarmuka dinamis yang meningkatkan perpindahan massa selama periode fluks tinggi O2 melintasi antarmuka. Fluks O2 yang tinggi ini disarankan untuk menurunkan tegangan antarmuka selama reaksi yang mengarah pada peningkatan luas antarmuka atau koefisien perpindahan massa atau keduanya.
Beberapa penelitian telah menunjukkan bahwa emulsifikasi spontan dapat terjadi selama periode perpindahan massa yang intens dari elemen aktif permukaan karena penurunan yang sangat nyata pada tegangan antarmuka antara dua cairan yang tidak dapat bercampur. Juga, untuk tegangan antarmuka kesetimbangan, kandungan O2 dan S (sulfur) dalam logam memainkan peran penting pada tegangan kesetimbangan yang diamati. Penambahan CaF2 dan Na2O menaikkan tegangan antarmuka tetapi penambahan MnO cenderung menurunkannya. Salah satu penelitian telah menunjukkan bahwa ketika fluks O2 menjadi lebih besar dari sekitar 0,1 g atom/sqm detik, tegangan antarmuka mendekati nilai yang mendekati nol. Ketika fluks O2 menjadi lebih rendah dari 0,01 g atom/sqm detik, tegangan antarmuka meningkat dengan cepat ke nilai yang mendekati tegangan kesetimbangan.
Kinetika defosforisasi telah dipelajari jauh lebih sedikit daripada keseimbangan P antara terak logam. Ada ketidaksepakatan apakah perpindahan massa dalam logam, terak atau keduanya mengontrol laju reaksi. Karena sifat reaksi, fenomena antarmuka dinamis tampaknya memiliki peran penting pada laju reaksi secara keseluruhan. Emulsifikasi spontan tampaknya terjadi ketika perpindahan massa cepat O2 terjadi pada antarmuka sistem terak logam. Hal ini menghasilkan penurunan yang substansial dalam tegangan antarmuka, sehingga meningkatkan luas reaksi dan laju keseluruhannya. Namun, perhitungan langsung dari perubahan area reaksi karena emulsifikasi spontan masih sangat sulit.




