Manufaktur perangkat medis dan bahan biokompatibel:Apa yang perlu diketahui pengembang produk

Pengobatan modern bergantung pada berbagai alat dan instrumen yang berbeda. Mulai dari pipa fleksibel hingga kain kasa hingga klem logam tahan lama dan kaki palsu, perangkat ini memiliki banyak bentuk. Sama seperti FDA yang mengatur bahan mana yang dapat digunakan dalam rantai pasokan makanan dan obat-obatan kita, mereka juga mengatur pengembangan dan produksi perangkat medis. Ini berarti bahwa bahan tertentu yang digunakan dalam aplikasi industri tidak dapat diterima untuk digunakan dalam produk yang berinteraksi dengan tubuh kita.
Pembatasan seputar bahan tertentu akan bervariasi menurut wilayah. Artinya, perangkat yang disetujui untuk digunakan di Amerika Serikat mungkin tidak memenuhi standar Uni Eropa.
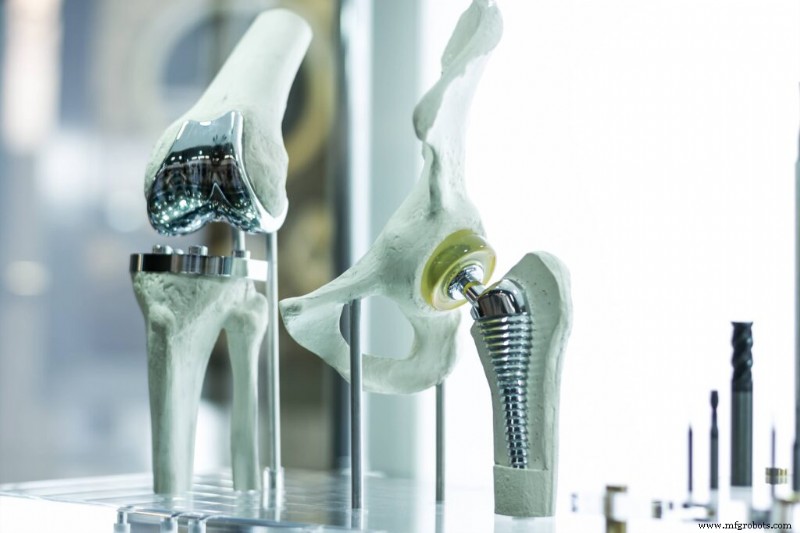
Meskipun tidak setiap perangkat medis membutuhkan bahan biokompatibel, banyak yang membutuhkannya. Jika perangkat ditujukan untuk penggunaan internal, perangkat ini akan menghadapi pengawasan yang lebih ketat daripada perangkat yang dapat membantu pembedahan atau kontak dengan kulit untuk sementara waktu. Contoh umum perangkat medis yang ditujukan untuk penggunaan internal meliputi alat pacu jantung, prostetik, stent, pinggul buatan, dan penggantian sendi lainnya.
Penting bagi tim pengembangan produk untuk mengetahui bahan biokompatibel mana yang paling sesuai untuk kebutuhan spesifik mereka guna melindungi kesehatan dan kesejahteraan pasien, mencapai kepatuhan berkelanjutan terhadap peraturan ketat, dan mengurangi risiko dan kewajiban. Berikut adalah beberapa pedoman utama dan prinsip dasar untuk pemilihan bahan perangkat medis.
Standar peraturan untuk bahan biokompatibel untuk perangkat medis
Bahan dan komponen yang digunakan oleh produsen perangkat medis harus memenuhi persyaratan kualitas dan kinerja yang ketat dari peraturan internasional ISO 10993, yang secara khusus mengatur biokompatibilitas. ISO 10993 menjabarkan pendekatan tentang cara melakukan mitigasi risiko dan pengujian kinerja untuk material perangkat secara konsisten dan seragam.
Pedoman ISO mendapat dukungan dari FDA. Pada bulan September 2020, agensi tersebut merilis dokumen panduan yang menawarkan saran tentang cara menerapkan peraturan ISO dan memastikan bahwa bahan yang disetujui FDA untuk perangkat medis sesuai dengan standar internasional.
Biokompatibilitas adalah subjek yang kompleks dan berkembang dengan beberapa definisi sederhana, dan pembaruan terbaru untuk pedoman ISO 10993 (10993-1:2018; diperbarui dari 10993-1:2009) mencerminkan perkembangan terbaru di lapangan. Mungkin perubahan paling signifikan dalam edisi terbaru ISO 10993 melibatkan bagaimana biokompatibilitas diuji.
Sementara versi sebelumnya menyediakan tes khusus untuk menilai biokompatibilitas dari berbagai jenis perangkat, standar saat ini berusaha untuk mengatasi banyak variabel yang terlibat dalam pembuatan perangkat medis melalui proses penilaian risiko, mitigasi, dan manajemen yang komprehensif. Hal ini memungkinkan standar untuk diterapkan dalam cakupan yang lebih luas dari konteks medis dan manufaktur yang dinamis.
Pembaruan ISO 10993 juga mencakup informasi tambahan atau yang diperbarui tentang perangkat medis kontak dan non-kontak, serta metode untuk mengevaluasi biokompatibilitas nanoteknologi, jalur gas, dan bahan yang dapat diserap.
Mendemonstrasikan biokompatibilitas umumnya dilakukan melalui proses tiga tahap:
- Tim produk mengembangkan Rencana Evaluasi Biologis (BEP), yang menguraikan risiko dan strategi yang diketahui untuk menguji atau mengurangi masalah ini. Dokumen ini memenuhi persyaratan ISO 10993-1 untuk penilaian risiko awal.
- Materi dan komponen perangkat diuji untuk mengatasi risiko yang diuraikan ini, yang dapat mencakup evaluasi faktor seperti bagaimana perangkat aus seiring waktu, toksisitas bahan, atau bagaimana perangkat beroperasi saat bersentuhan dengan cairan. Seringkali, berbagai jenis pengujian dan kontrol desain untuk perangkat medis diperlukan untuk memastikan perangkat berfungsi sebagaimana mestinya.
- Tim produk menggabungkan hasil pengujian dan analisis data ke dalam Laporan Evaluasi Biologis (BER), yang kemudian mereka serahkan ke FDA untuk disetujui.
Tantangan biokompatibilitas tambahan
Selain mencapai kepatuhan terhadap peraturan ISO dan FDA, desain perangkat medis biokompatibel dapat menimbulkan tantangan tambahan bagi tim produk. Tim pengembangan produk perangkat medis sering kali memiliki persyaratan fungsional atau terkait desain tertentu yang harus mereka patuhi, dan menyelaraskan persyaratan ini dengan batasan material dapat menjadi proses yang memakan waktu dan intensif. Faktanya, bukan hal yang aneh jika persyaratan pelanggan mengharuskan sekumpulan properti material yang saling bertentangan atau eksklusif — dan tim produk harus melakukan penelitian yang mengarah pada kompromi yang dapat diterima.
Tantangan utama lainnya melibatkan jadwal produksi. Pengujian yang diperlukan untuk penilaian toksikologi dan biokompatibilitas tidak menghasilkan hasil lulus atau gagal yang sederhana; melainkan, evaluasi ini secara kolektif menciptakan demonstrasi kepatuhan atau rekomendasi untuk penelitian dan evaluasi lebih lanjut. Karena ini memerlukan pendekatan yang menyeluruh dan terdokumentasi dengan baik, proses sertifikasi dan persetujuan untuk alat kesehatan tidak dapat dilakukan secara terburu-buru. Tim produk yang sukses adalah mereka yang memiliki keterampilan dan keahlian untuk memenuhi persyaratan pelanggan saat beroperasi sesuai dengan peraturan ISO dan FDA.
Pertimbangan utama untuk memilih bahan biokompatibel yang tepat

Ada banyak variabel dan faktor yang perlu dipertimbangkan saat merancang dan membuat perangkat medis biokompatibel, dan detail spesifik tentu saja akan bervariasi berdasarkan aplikasinya. Namun, memilih bahan yang tepat adalah yang terpenting, karena para peneliti telah menemukan bahwa 30-40% dari penarikan perangkat disebabkan oleh pilihan material yang tidak tepat. Berikut adalah tiga pertimbangan utama untuk tim produk:
- Ketersediaan bahan: Jika desain alat kesehatan termasuk bahan yang langka atau sulit didapat, solusi alternatif mungkin diperlukan. Ini membantu menjaga biaya per unit tetap rendah dan memastikan bahwa perangkat dapat mencapai pasar sesuai jadwal.
- Proses pembuatan :Kebutuhan material suatu alat kesehatan atau komponennya akan membantu menentukan metode atau metode produksi yang optimal. Cetakan injeksi, misalnya, adalah cara yang cepat dan hemat biaya untuk membuat sejumlah besar komponen plastik presisi dengan permukaan akhir yang baik, tetapi bisa sangat mahal untuk produksi volume rendah. Pemesinan CNC, di sisi lain, memiliki sedikit batasan material tetapi beberapa batasan geometris yang signifikan. Demikian juga, perkembangan teknologi manufaktur aditif memungkinkan produksi yang lebih cepat dan kustomisasi yang lebih besar — kualitas yang sangat berharga mengingat pergeseran skala besar sektor medis menuju perawatan yang berpusat pada pasien — meskipun perlu dicatat bahwa baik mesin CNC maupun manufaktur aditif kompatibel dengan produk yang relatif terbatas. berbagai bahan.
- Perlu sterilisasi :Beberapa alat dan perlengkapan medis, seperti jarum suntik dan selang infus, harus disterilkan sebelum dapat diedarkan kembali untuk digunakan. Dalam istilah desain, ini berarti perangkat harus memiliki ketahanan material terhadap proses sterilisasi. Mengetahui sejak dini apakah suatu perangkat akan memiliki persyaratan sterilisasi — selain metode sterilisasi yang akan digunakan — adalah kunci untuk menghindari revisi dan pengujian yang mahal.
Mempertahankan proses desain yang efisien selama pengembangan produk perangkat medis
Mengingat bahwa pengujian dan persetujuan biokompatibilitas memerlukan evaluasi berkelanjutan, tim pengembangan produk kemungkinan perlu menyesuaikan atau memikirkan kembali proses desain mereka berdasarkan temuan mereka.
Ada beberapa cara struktural di mana tim dapat merampingkan proses desain mereka. Mempertahankan basis data bahan yang akurat yang mencakup informasi terkait hasil pengujian, toksikologi atau karsinogenisitas bahan, dan karakteristik lain yang ditetapkan oleh ISO 10993, adalah langkah pertama untuk membuat arsip data historis yang dapat dirujuk kembali dalam upaya desain di masa mendatang . Melakukannya tidak hanya membantu meningkatkan efisiensi modifikasi selama proses desain, tetapi juga membantu tim desain tetap mengenal berbagai bahan yang relevan dengan persyaratan biokompatibilitas dan fungsionalitas perangkat.
Jika bahan komponen telah dipilih tetapi geometri bagian belum diselesaikan, pengujian plak adalah teknik yang memungkinkan tim untuk tetap produktif dan efisien. Teknik ini melibatkan pembuatan beberapa plakat kecil melalui metode pembuatan yang akan digunakan untuk membuat produk akhir. Plak tersebut kemudian menjalani pengujian biokompatibilitas — termasuk pengujian kimia dan menentukan bagaimana bahan terurai dari waktu ke waktu — sementara pengembang produk menyelesaikan desain bagian. Hal ini membantu membangun dasar untuk evaluasi selanjutnya dan dapat mempercepat proses persetujuan peraturan.
Memilih mitra manufaktur yang tepat untuk pekerjaan tersebut
Proses terbaru yang terkandung dalam ISO 10993 terbaru berupaya meminimalkan pengujian yang tidak perlu sambil tetap menjamin bahwa tim produk dapat memperhitungkan seberapa relevan faktor seperti desain perangkat, karakteristik fisik dan kimia bahan perangkat, dan bahkan proses manufaktur dapat memengaruhi kualitas perangkat dan seberapa baik mereka dapat memenuhi kebutuhan pasien. Proses desain, pengembangan, dan regulasi yang berat yang diperlukan untuk pembuatan perangkat medis yang efektif dapat menghadirkan tantangan yang signifikan bagi tim produk, itulah sebabnya sangat bermanfaat untuk bermitra dengan produsen yang sudah teruji seperti Fast Radius.
Fast Radius adalah platform manufaktur digital sesuai permintaan yang inovatif dengan pengalaman signifikan bekerja dengan tim desain perangkat medis untuk menghadirkan produk yang aman dan andal ke pasar. Keterampilan dan teknik kami telah digunakan untuk membuat prostetik canggih, model bedah yang sangat presisi, dan banyak lagi, dan tim kami siap memberikan layanan konsultasi dan dukungan 360 derajat mulai dari tahap desain dan pembuatan prototipe hingga produksi dan pemenuhan. Siap untuk memulai? Hubungi tim kami hari ini.
Pelajari lebih lanjut tentang rangkaian lengkap kemampuan kami — termasuk solusi untuk perusahaan perusahaan — dengan mengunjungi pusat pembelajaran Fast Radius.
Siap membuat suku cadang Anda dengan Radius Cepat?
Mulai kutipan Anda






