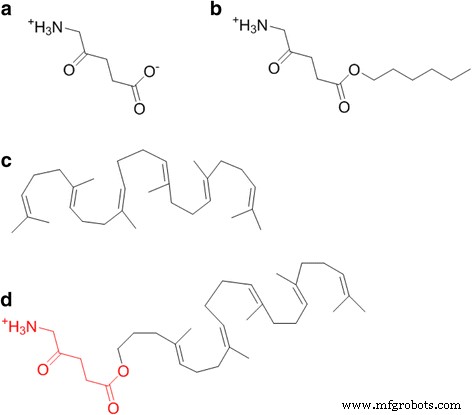
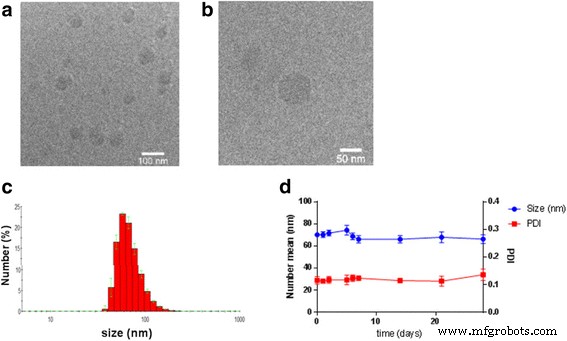
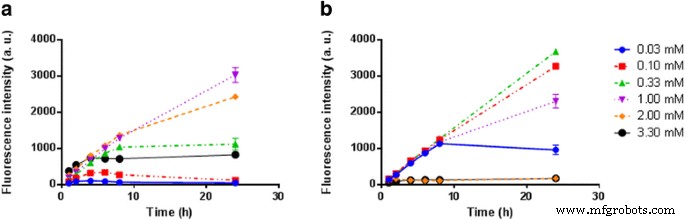
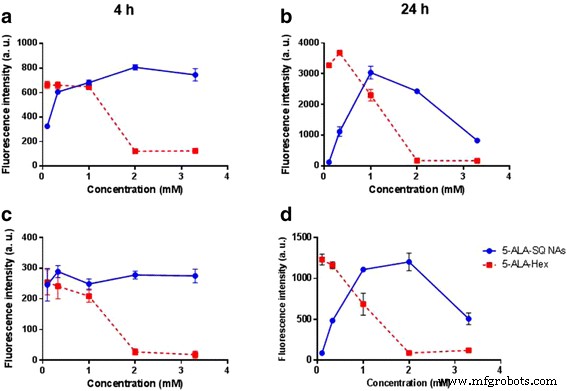
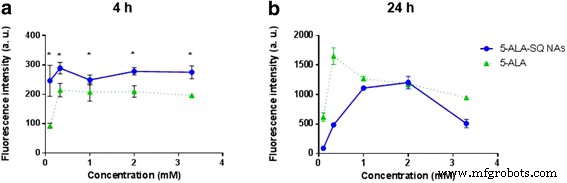
Dalam studi pembuktian konsep in vitro ini, strategi kimia konvergen digunakan untuk mensintesis blok bangunan 5-ALA-SQ dari squalene dan 5-ALA. NA 5-ALA-SQ disiapkan dengan nanopresipitasi spontan dalam air. NA bersifat monodispersi dan stabil dengan ukuran rata-rata 70 nm, indeks polidispersitas 0,12, potensi positif 36 mV, dan pemuatan 5-ALA tinggi 26%. Produksi ppIX dievaluasi secara in vitro dalam dua garis sel kanker dengan mengukur peningkatan fluoresensi dari waktu ke waktu dan dibandingkan dengan 5-ALA dan 5-ALA-Hex. Hasil penelitian menunjukkan bahwa SQ-ALA NAs sangat efisien dalam menginduksi produksi PpIX pada sel kanker tipe PC3 dan U87MG. Mereka mengungguli 5-ALA-Hex dalam induksi fluoresensi pada konsentrasi yang lebih tinggi pada waktu inkubasi 4 dan 24 jam secara in vitro; namun, dibandingkan dengan 5-ALA, mereka menunjukkan induksi fluoresensi yang unggul pada waktu inkubasi yang lebih singkat. Dalam ruang lingkup dengan temuan ini, kita dapat menyimpulkan bahwa 5-ALA-SQ NAs menghadirkan solusi nanoteknologi yang menarik untuk mengatasi kelemahan farmakokinetik 5-ALA. Lebih lanjut, eksperimen in vivo akan mengevaluasi potensinya untuk pengiriman sistemik 5-ALA untuk terapi fluoresensi PD dan PDT tumor.
Metode/Eksperimental
Reagen dibeli dari pemasok komersial Sigma-Aldrich (Bucks, Swiss) dan Acros Organics (Basel, Swiss) dan digunakan tanpa pemurnian lebih lanjut. Pelarut NMR terdeuterasi diperoleh dari Cambridge Isotop Laboratories (Tewksbury, USA). Tetrahidrofurana (THF) dan diklorometana (CH2 Kl2 ) diperoleh dari sistem pengeringan berbasis kolom alumina Anhydrous Engineering. Semua pelarut lain yang digunakan adalah kelas HPLC. N,N-dimetilformamida (DMF), metanol (CH3 OH), dietil eter (Et2 O) dan aseton dibeli dari Sigma-Aldrich (Buchs, Swiss). Etil asetat (AcOEt) dibeli dari Biosolve (Dieuze, Prancis); asetonitril (CH3 CN) dipasok oleh Reagen Carlo Erba (Balerna, Swiss). Heksana 95% dari n-heksana dibeli dari Fisher Chemical (Basel, Swiss). Air yang digunakan untuk persiapan dideionisasi oleh sistem air laboratorium Milli-Q (Millipore, Molsheim, Prancis). Reaksi kimia dilakukan menggunakan septa jarum suntik standar dengan tekanan positif argon untuk memastikan kondisi anhidrat.
Kromatografi lapis tipis (KLT) dilakukan dengan pelat silika yang didukung aluminium (Merck-Keiselgel 60 F254) dengan fase gerak yang sesuai dan divisualisasikan menggunakan lampu fluoresensi UV (254 dan 366 nm) dan/atau dikembangkan dengan ninhidrin, 20% sulfat asam, atau asam fosfomolibdat (PMA). Kromatografi flash dilakukan pada mesin PuriFlash® 4100 otomatis dari Interchim (Montlucon, Prancis) menggunakan kolom silika Interchim puriFlash® HP 30 μm yang dilengkapi dengan detektor PDA (200–800 nm) dan pengumpul pecahan otomatis. Profil elusi dipantau menggunakan software Flash Interchim versi 5.0x. Kolom HPLC semi-preparatif dilakukan pada Waters Symmetry 300TM - 5 μm (19 × 150 mm), kolom C8 (Baden-Dättwil, Swiss). UPLC analitik dilakukan menggunakan kolom Macherey-Nagel EC50/2 Nucleodur Gravity 1,8 m (50 × 2.1 mm) yang dipasang pada sistem air yang dilengkapi dengan detektor PDA Perairan (Baden-Dättwil, Swiss). Penyangga A = CH3 CN + 0,1% Asam format) dan buffer B = H2 O + 0,1% Asam format. Laju aliran =400,0 μL/mnt pada 25 °C.
1
H dan
13
Spektrum C NMR direkam pada spektrometer Varian Gemini 300 MHz, Varian Innova 500 MHz, atau Bruker Avance III Cryo 600 MHz pada 298 K. Pergeseran kimia (δ) dinyatakan dalam bagian per juta (ppm) dan konstanta kopling (J) dinyatakan dalam hertz (Hz). s untuk singlet, d untuk doublet, dd untuk doublet doublet, t untuk triplet, q untuk quartet, dan m untuk multiplet. Puncak pelarut sisa digunakan sebagai referensi internal untuk pergeseran kimia proton dan karbon. Spektrum NMR diproses dengan paket perangkat lunak Mnova versi 10.0.2. Spektrometri massa resolusi rendah (LRMS) dilakukan pada instrumen HTS PAL-LC10A – API 150Ex dalam ESI (mode positif). Spektrometri massa resolusi tinggi (HRMS) dilakukan pada instrumen QSTAR Pulsar (AB/MDS Sciex) dalam ESI (mode positif). Struktur kimia digambar dan diberi nama sesuai nomenklatur IUPAC menggunakan paket perangkat lunak ChemBioDraw Ultra versi 14.0.0.117. pH diukur pada pH meter Metrohm 691 menggunakan elektroda ujung tombak (Zofingue, Swiss), dikalibrasi dengan buffer Metrohm. Analisis statistik dilakukan menggunakan perangkat lunak GraphPad Prism 6, 2016, (GraphPad Software). P nilai < 0,05 dianggap signifikan secara statistik.
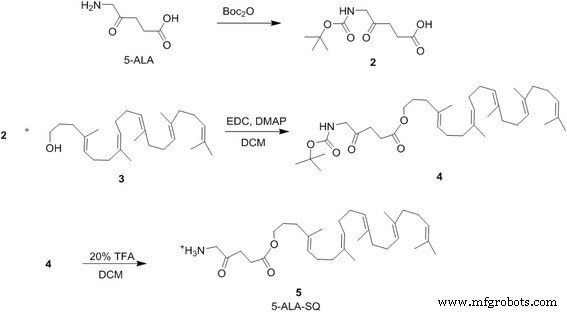
Sintesis Blok Bangunan SQ-ALA
5-(tert-Butoxycarbonylamino)-4-oxopentanoic Acid (2)
Boc-5-ALA disintesis menurut prosedur yang diterbitkan. Data spektroskopi identik dengan literatur [56].
1
H NMR (600 MHz, DMSO-d6) 12,12 (s, 1H), 7,06 (t, J = 5.9 Hz, 1H), 3,76 (d, J = 5.9 Hz, 2H), 2,61 (t, J = 6.6 Hz , 2H), 2,40 (t, J = 6,5 Hz, 2H), 1,38 (s, 9H).
13
C NMR (151 MHz, DMSO) 206.62, 174.07, 156.21, 78.54, 49.97, 40.38, 40.24, 40.11, 39.97, 39.83, 39.69, 39.55, 34.22, 28.64. [M+H]
+
232.1, ditemukan 232.7.
(4E,8E,12E,16E)-4,8,13,17,21-pentamethyldocosa-4,8 ,12,16,20-pentaen-1-ol (3)
Alkohol squalene 3 disintesis dari squalene dalam empat langkah sintetik dengan hasil 23,7% sebagai minyak tidak berwarna menurut prosedur yang dilaporkan [49].
1
H NMR (300 MHz, CDCl3 ) 5,17-5,06 (m, 5H, CH), 3,62 (q, J =6,3 Hz, 2H, CH2 -OH), 2,17 – 1,92 (m, 18H, CH2 ), 1,67 (dtk, 3H, CH3 ), 1,59 (m, 17 H, CH3 dan CH2 ).
13
C NMR (75 MHz, CDCl3 ) 135.35, 135.17, 135.14, 134.81, 131.49, 125.05, 124.64, 124.60, 124.47, 63.07, 39.98, 39.95, 39.89, 36.24, 30.92, 28.48, 26.98, 26.88, 26.78, 25.94, 17.92, 16.28. LRMS (ESI):m/z dihitung untuk [M+NH4 <
+
404.4, ditemukan 404.8.
(4E,8E,12E,16E)-4,8,13,17,21-pentamethyldocosa-4,8 ,12,16,20-pentaen-1-yl 5-((tert-butoxy karbonil)amino)-4-oxopentanoate (4)
Alkohol squalene (3 ) (100 mg, 0,26 mmol), EDC (74 mg, 0,38 mmol) dan DMAP (94 mg, 0,78 mmol), dan 5-(tert-Butoxycarbonylamino)-4-asam oksopentanoat (2) (77 mg, 0,34 mmol) dilarutkan dalam DCM (15 mL). Setelah diaduk semalaman pada suhu kamar, pelarut diuapkan pada tekanan tereduksi dan produk kasar dimurnikan dengan kromatografi Flash menggunakan gradien DCM/etil asetat (EA) menghasilkan minyak tidak berwarna (108 mg, 0,18 mmol, 70%).
1
H NMR (300 MHz, CDCl3 ) 5,31 – 5,20 (br s, 1H), 5,13 – 5,07 (m, 5H), 4,09 – 3,95 (m, 4H), 2,75 – 2,53 (m, 4H), 2,02 – 1,95 (m, 20H), 1,64 ( s, 3H), 1,63 – 1,50 (m, 19H), 1,41 (dt, 9H).
13
C NMR (75 MHz, CDCl3) 204.46, 172.65, 135.30, 135.16, 135.09, 133.75, 131.43, 125.34, 124.60, 124.57, 124.48, 124.45, 64.81, 50.53, 39.96, 39.93, 39.87, 35.92, 34.56, 28.52 , 28.43, 28.24, 28.02, 26.97, 26.86, 25.92, 23.11, 17.90, 16.25, 16.21, 16.06. LRMS (ESI):m/z dihitung untuk [M+NH4 <
+
617.5, ditemukan 617.8.
Garam asam trifluoroasetat dari 5-amino-(((4E,8E,12E,16E)-4,8,13 ,17,21-pentamethyldocosa-4,8,12,16,20-pentaen-1-yl)oxy)-4-oxopentanoate (5)
Senyawa 4 (34 mg, 57 mmol) dilarutkan dalam DCM (2,0 mL). Asam trifluoroasetat (TFA) (200 L) ditambahkan dan campuran reaksi diaduk pada suhu kamar. Setelah 10 menit, pelarut diuapkan dalam vakum pada suhu rendah dan sisa-sisa TFA dihilangkan dengan evaporasi bersama dengan EA (3 × 10 mL). Produk mentah dimurnikan dengan RP-HPLC menggunakan H2 . penuh Gradien O/AcN (0,025% TFA) menghasilkan minyak tidak berwarna (25 mg, 74%). %).
1
H NMR (300 MHz, CDCl3 ) 5,31 – 5,20 (br s, 1H), 5,13 – 5,07 (m, 5H), 4,09 – 3,95 (m, 4H), 2,75 – 2,53 (m, 4H), 2,02 – 1,95 (m, 20H), 1,64 ( s, 3H), 1,63 – 1,50 (m, 19H). LRMS (ESI):m/z dihitung untuk [M+H]
+
500,4, ditemukan 500,6.
Persiapan Rakitan Nano
NA disiapkan oleh nanopresipitasi dijelaskan secara rinci di tempat lain [20]. Secara singkat, blok penyusun 5 (1,2 mg, 2,0 μmol) dilarutkan dalam 50/50 V /V campuran aseton/etanol (500 L). Fase organik kemudian ditambahkan tetes demi tetes menggunakan jarum suntik mikro ke dalam air MilliQ (1,25 mL) pada 100 μL/menit dengan pengadukan magnetik. Setelah 5 menit di bawah pengadukan, batang pengaduk magnet dihilangkan dan pelarut organik dan kelebihan air dihilangkan menggunakan rotary evaporator pada 30 °C. Konsentrasi akhir rakitan nano adalah 2,00 mM.
Karakterisasi NA 5-ALA-SQ
Pemuatan 5-ALA dari 5-ALA.SQ NA dihitung dari kontribusi masing-masing bobot molekul 5-ALA dan konjugat 5-ALA-SQ sebagai berikut [19]:
$$ \mathrm{Memuat}\ \left(\%\right)=\frac{\mathrm{MW}\ \left(5-\mathrm{ALA}\right)}{\mathrm{MW}\left(5 -\mathrm{ALA}-\mathrm{SQ}\right)}\times 100 $$
Diameter hidrodinamik NA diukur dengan hamburan cahaya dinamis (DLS) menggunakan instrumen NANO ZS dari Malvern (Worcestershire, Inggris) yang menjalankan perangkat lunak ZetaSizer 7.01. Analisis dilakukan dengan 4 mW He-Ne Laser (633 nm) pada sudut hamburan 173° pada 25 °C dalam kuvet mikro polistirena (PS) dari Brand (Wertheim, Jerman). Potensi zeta (ZP) ditentukan menggunakan instrumen Nano ZS yang sama dari Malvern dalam sel kapiler terlipat DTS 1070 dari Malvern. Distribusi ukuran dan ukuran diameter rata-rata dihitung dari data. Stabilitas NA yang disimpan pada 4 °C diuji oleh DLS pada titik waktu reguler selama periode 1 bulan.
Morfologi NA dinilai dengan mikroskop elektron transmisi kriogenik (cryo-TEM) menggunakan TECNAI® G
2
Mikroskop sphera (FEI, Thermo Fisher Scientific) dilengkapi dengan kamera digital TCL resolusi tinggi 2000 x 2000 piksel (Gräfelfing, Jerman). Sampel es vitrifikasi disiapkan menggunakan cryo-plunger Virtobot (FEI, Thermo Fisher Scientific). NA (2.0 μL, 2.0 mM) diterapkan pada kisi Quantifoil Cu/Rh 200 mesh R3.5/1 (SPI, West Chester, USA) dan divitrifikasi menggunakan etana cair.
Budaya Sel
Sel kanker prostat manusia PC3 (ATTC® CRL-1435™) dan sel glioblastoma manusia U87MG (ATTC® HTB-14™) ditumbuhkan dan dipelihara melalui jalur serial dalam campuran nutrisi F-12K (21127-022, Thermo Fisher Scientific) atau minimum Media Esensial (31095-029, Thermo Fisher Scientific), masing-masing. Media sel dilengkapi dengan serum betis janin (10%, CVFSVF00-01, Eurobio), streptomisin (100 L/mL), dan penisilin (100 IU/mL, 15140-122, Thermo Fisher Scientific). Sel dibudidayakan pada suhu 37 °C dalam atmosfer yang dilembabkan yang mengandung 95% udara dan 5% CO2.
Pengukuran Kinetik Fluoresensi PpIX In Vitro
Sel kanker prostat manusia PC3 (12.000 sel/sumur) dan sel glioblastoma U87MG (10.000 sel/sumur) diunggulkan dalam pelat 96-sumur (pelat hitam bawah bening, 3603, Corning). Hari berikutnya, sel-sel diekspos ke peningkatan konsentrasi 5-ALA-SQ NAs, 5-ALA-Hex, dan 5-ALA dalam media bebas serum. Fluoresensi PpIX direkam dengan pembaca pelat (Safire, Tecan, Swiss) pada titik waktu yang berbeda. Panjang gelombang eksitasi diatur ke 405 nm dan panjang gelombang emisi ke 630 nm. Nilai rata-rata dan s.d. untuk setiap konsentrasi pada setiap titik waktu per piring dikurangi dengan nilai referensi (tanpa perlakuan) dan diplot untuk setiap baris sel.